في الأول ، استخدم الأطباء في الولايات المتحدة أداة كريسبر لعلاج المرضى الذين يعانون من اضطراب وراثي
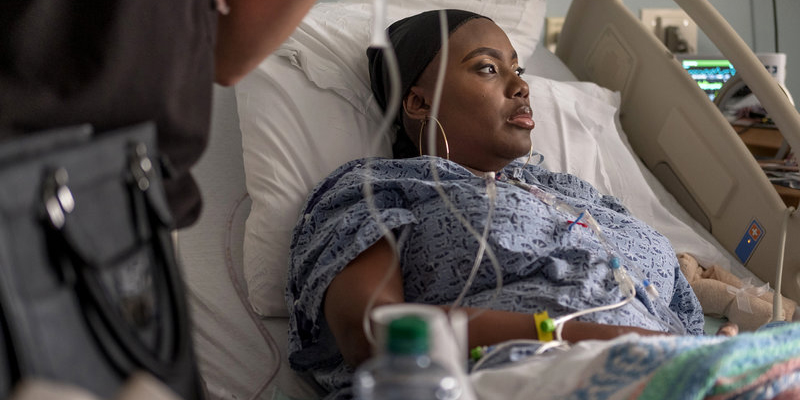
فيكتوريا غراي، 34 عامًا، من فورست، ميسيسيبي، تطوعت لإحدى أكثر التجارب الطبية انتظارًا منذ عقود: المحاولة الأولى لاستخدام تقنية تعديل الجينات كريسبر لعلاج اضطراب وراثي في الولايات المتحدة.
لأول مرة، استخدم الأطباء في الولايات المتحدة تقنية تعديل الجينات القوية كريسبر لمحاولة علاج مريض يعاني من اضطراب وراثي.
“من المذهل حقًا مدى التقدم الذي أحرزناه”، تقول فيكتوريا غراي، 34 عامًا، من فورست، ميسيسيبي. “إنه أمر رائع”، قالت لـ NPR في مقابلة حصرية بعد خضوعها للعلاج التاريخي لمرض فقر الدم المنجلي.
غراي هي أول مريضة يتم التعرف عليها علنًا كمشاركة في دراسة تختبر استخدام كريسبر لعلاج مرض وراثي.
“كنت دائمًا آمل أن يظهر شيء ما”، تقول من سرير المستشفى في معهد سارة كانون للأبحاث في ناشفيل، تينيسي، حيث تلقت حقنًا بمليارات الخلايا المعدلة وراثيًا. “إنه وقت مناسب للشفاء.”
لكن ربما سيستغرق الأمر أشهرًا، إن لم يكن سنوات، من المراقبة الدقيقة لغراي والمرضى الآخرين قبل أن يعرف الأطباء ما إذا كان العلاج آمنًا ومدى فعاليته في مساعدة المرضى.
يؤثر مرض فقر الدم المنجلي على ملايين الأشخاص حول العالم. حوالي 100,000 شخص في الولايات المتحدة، ومعظمهم، مثل غراي، من الأمريكيين الأفارقة. يتسبب عيب وراثي في إنتاج النخاع العظمي لبروتين معيب يجعل خلايا الدم على شكل منجل، صلبة ولزجة. هذه الخلايا المشوهة تعلق داخل الأوعية الدموية ولا تحمل الأكسجين بشكل طبيعي، مما يسبب مجموعة من المضاعفات المؤلمة وغالبًا ما تقصر العمر.
“إنه أمر فظيع”، تقول غراي. “عندما لا تستطيع المشي أو رفع ملعقة لتطعيم نفسك، يصبح الأمر صعبًا جدًا.”
في الدراسة، يستخدم الأطباء خلايا مأخوذة من نخاع العظم للمرضى تم تعديلها وراثيًا باستخدام كريسبر لجعلها تنتج بروتينًا يتم إنتاجه عادة من قبل الأجنة والرضع لفترة قصيرة بعد الولادة.
الأمل هو أن هذا البروتين سيعوض عن البروتين المعطل الذي يسبب مرض فقر الدم المنجلي وسيمكن المرضى من العيش بشكل طبيعي لبقية حياتهم.
“من المثير أن نرى أننا قد نكون على وشك علاج فعال جدًا للمرضى المصابين بفقر الدم المنجلي”، يقول د. ديفيد ألتشولر، نائب الرئيس التنفيذي للبحوث العالمية وكبير العلماء في شركة فيرتكس فارماسيوتيكالز في بوسطن. تجري فيرتكس الدراسة بالتعاون مع كريسبر ثيرابيوتيكس في كامبريدج، ماساتشوستس.
أعلنت كريسبر ثيرابيوتيكس عن علاج أول متطوع يوم الاثنين لكنها لم تذكر اسم المريض. ومع ذلك، حصلت NPR على وصول حصري لغراي.
“لقد كان الأشخاص المصابون بمرض فقر الدم المنجلي ينتظرون طويلًا علاجات تسمح لهم فقط بالعيش حياة طبيعية”، يقول ألتشولر.
“هذا أمر كبير جدًا”، يوافق د. حيدر فرانغول، المدير الطبي لهيماتولوجيا/أورام الأطفال في المعهد حيث تطوعت غراي. “قد يستفيد العديد من المرضى من هذا.”
مركز فرانغول، سارة كانون، يجري الدراسة في مركز HCA للرعاية الصحية TriStar Centennial الطبي في ناشفيل، وهو واحد من ثمانية مواقع تجنيد للمرضى للبحث في الولايات المتحدة وكندا وأوروبا. سيتم تسجيل ما يصل إلى 45 مريضًا تتراوح أعمارهم بين 18 و35 عامًا.
كما يشجع الأطباء والعلماء والأخلاقيون الحيويون الآخرين على المشاركة.
“هذه لحظة مثيرة في الطب. تعد كريسبر بالقدرة على تعديل الجينوم البشري وبدء معالجة الأمراض الوراثية مباشرة”، تقول لوري زولوث، أخصائية الأخلاقيات الحيوية في جامعة شيكاغو.
لكن زولوث حذرة أيضًا. فهي قلقة من أن هذه الدراسات وغيرها التي بدأت باستخدام كريسبر لم تمر بطبقة إضافية من التدقيق من قبل لجنة خبراء خارجية شكلتها المعاهد الوطنية للصحة.
“هذه تقنية جديدة تمامًا”، تقول زولوث. “يبدو أنها تعمل بشكل جيد جدًا في الحيوانات وفي الأطباق المخبرية. إنه أمر غير معروف تمامًا كيف ستعمل في البشر. هناك الكثير من المجهول. قد يجعلك المرض أسوأ.”
يعترف فرانغول بأن هناك دائمًا مخاطر مع العلاجات التجريبية. لكنه يقول إن البحث سيتم ببطء وحذر شديد مع مراجعة دقيقة من إدارة الغذاء والدواء ولجان استشارية أخرى.
“نحن حذرون جدًا بشأن كيفية إجراء هذه التجربة بطريقة منهجية جدًا لمراقبة المرضى بعناية لأي مضاعفات مرتبطة بالعلاج”، يقول.
من جهتها، تقول غراي إنها تفهم المخاطر. كما تقول إنها تعرف أن الدراسة هي خطوة أولى وأن المرضى الآخرين قد يرون الفوائد بعد سنوات فقط.
“هذا يعطيني الأمل إذا لم يعطني شيئًا آخر”، تقول غراي.
من المحتمل أن يستغرق الأمر عدة أشهر قبل أن يكتشف الأطباء العلامات الأولى لما إذا كانت الخلايا المعدلة وراثيًا تنتج مستويات مفيدة من البروتين، وسيستغرق وقتًا أطول لمعرفة ما إذا كانت الخلايا تحسن صحة المرضى. ومن المرجح أن يستغرق الأمر سنوات عديدة لمعرفة ما إذا كانت الفوائد ستدوم مدى الحياة، كما هو مأمول.
تم تشخيص غراي، المتزوجة ولديها أربعة أطفال، بمرض فقر الدم المنجلي عندما كانت رضيعًا وبدأت بالبكاء أثناء الاستحمام. أحد الأعراض الرئيسية هو الألم الشديد والمُعيق.
مثل العديد من مرضى فقر الدم المنجلي، منعت أعراضها غراي من عيش حياة كاملة. لم تستطع اللعب مثل الأطفال الآخرين، وكانت خائفة من السفر واضطرت للتخلي عن أحلامها بأن تصبح طبيبة أو ممرضة.
“أحيانًا أشعر وكأن الصواعق تضرب صدري وألم حاد في كل جسدي”، تقول غراي. “أحيانًا سأكون منحنية وأبكي، غير قادرة على فعل أي شيء لنفسي.”
تزيد خلايا الدم المعيبة أيضًا من خطر العدوى وإلحاق الضرر بالأعضاء الحيوية مثل القلب. كما يمكن أن تسبب جلطات دماغية تهدد الحياة. العديد من مرضى فقر الدم المنجلي لا يعيشون بعد الأربعين. لقد تضرر قلب غراي بالفعل، وهذا يترك أثرًا نفسيًا إضافيًا.
“إنه أمر مخيف”، تقول، واصفة كيف أثر مرضها على ابنها الأكبر، جماريوس، 12 عامًا.
“هو أكبر سنًا، لذا يفهم. لذلك بدأ يتصرف بشكل غير لائق في المدرسة. وأخبرتني معلمته، ‘أعتقد أن جماريوس يتصرف هكذا لأنه يعتقد حقًا أنك ستموتين’ “، تقول غراي وهي تكتم دموعها.
يمكن لبعض المرضى الحصول على زرع نخاع العظم، لكن تلك الإجراءات متعبة وخطيرة إذا هاجمت خلايا جهاز المناعة المنتجة من النخاع المزروع أجسامهم. ومعظم مرضى فقر الدم المنجلي إما لا يملكون أو لا يجدون متبرعًا مناسبًا.
“إنه أمر صعب جدًا”، تقول غراي. “كان ديني هو ما أبقاني مستمرة.”
عندما كانت تفكر في زرع نخاع العظم، سمعت عن تجربة كريسبر وأسرعت للتطوع.
“كنت أعلم دائمًا أن شيئًا ما يجب أن يحدث وأن الله كان لديه شيء مهم معد لي”، تقول غراي. “شعرت أن هذا كان قدرًا. كان شعورًا مذهلًا.”
تمكن تقنية كريسبر العلماء من إجراء تغييرات دقيقة جدًا في الحمض النووي، مما يثير الآمال في أنها ستؤدي إلى طرق جديدة للوقاية من الأمراض وعلاجها.
“لتقنية كريسبر العديد من الاستخدامات المحتملة في المستقبل، ليس فقط في اضطرابات الدم”، يقول فرانغول.
بدأ الأطباء بالفعل في استخدامها لمحاولة علاج السرطان، في الغالب في الصين. تم علاج مريضين على الأقل في الولايات المتحدة من السرطان، في دراسة بجامعة بنسلفانيا في فيلادلفيا.
في وقت لاحق من هذا العام، يخطط الأطباء في بوسطن لاستخدام كريسبر لتحرير خلايا شبكية المرضى، على أمل استعادة الرؤية لدى المرضى الذين يعانون من شكل وراثي من العمى.
أعلنت الشركات الراعية لدراسة فقر الدم المنجلي في وقت سابق من هذا العام أنها استخدمت كريسبر لعلاج أول مريض باضطراب دم مشابه، بيتا ثلاسيميا، في ألمانيا.
يوم الاثنين، كشفت كريسبر ثيرابيوتيكس أيضًا عن أول مؤشر على أن النهج قد يكون ناجحًا لمرض بيتا ثلاسيميا. بدأت خلايا المريض المعدلة بالعمل في نخاع العظم، وفقًا لبيان الشركة الصحفي.
علاوة على ذلك، لم يتطلب المريض نقل دم لأكثر من أربعة أشهر، حسبما تقول الشركة. عادة ما يحتاج مرضى بيتا ثلاسيميا إلى نقل دم منتظم لعلاج حالتهم.
تسبب كل من بيتا ثلاسيميا ومرض فقر الدم المنجلي عيوبًا جينية تسبب مشاكل في بروتين يسمى الهيموغلوبين. تستخدم خلايا الدم الحمراء الصحية الهيموغلوبين لنقل الأكسجين في جميع أنحاء الجسم.
تحمل خلايا الدم الحمراء لمرضى فقر الدم المنجلي هيموغلوبين معيب يشوه الخلايا ولا ينقل ما يكفي من الأكسجين. الأمل هو أن شكلًا آخر من الهيموغلوبين، يُعرف باسم هيموغلوبين الجنين، سيعوض عن البروتين المعطل.
ينتج هيموغلوبين الجنين من قبل الأجنة في الرحم لتوفير الأكسجين. في معظم الناس، يتوقف إنتاج هيموغلوبين الجنين بعد الولادة مباشرة.
“بمجرد أن يولد الطفل، يتم تشغيل مفتاح”، يقول فرانغول. “إنه جين يخبر خلايا الدم الحمراء — خلايا نخاع العظم التي تنتج خلايا الدم الحمراء — بالتوقف عن إنتاج هيموغلوبين الجنين.”
يبدأ علاج كريسبر هذا باستخراج خلايا نخاع العظم من دم المرضى. ثم يستخدم علماء الشركة كريسبر لتحرير جين في الخلايا لجعلها تنتج هيموغلوبين الجنين.
“هذا سيساعد الخلايا على إنتاج المزيد من هيموغلوبين الجنين ويجعلها أكثر سعادة وصحة”، يقول فرانغول.
ثم يخضع المرضى لنفس نوع العلاج الكيميائي القاسي المقدم كجزء من زرع نخاع العظم القياسي. هذا يزيل الخلايا الحالية التي تحمل العيب الجيني. لكن بدلاً من تلقي خلايا جديدة من متبرع، يحصل المرضى على مليارات من خلاياهم الخاصة التي تم تعديلها باستخدام كريسبر.
الأمل هو أن يوفر هذا خيارًا علاجيًا لجميع المرضى، بما في ذلك أولئك الذين لا يمكنهم العثور على متبرع متطابق. ومن المأمول أن يكون النهج أكثر أمانًا لأن الخلايا تأتي من نخاع المرضى أنفسهم. لذلك، لا ينبغي أن تهاجم أجسام المرضى، كما يقول فرانغول.
“هذا يفتح الباب للعديد من المرضى لعلاج مرضهم وتعديله ليصبح خفيفًا” وتجنب “الآثار الجانبية الطويلة المدى المروعة لمرض فقر الدم المنجلي”، كما يقول.
بالنسبة لغراي، كانت العملية أحيانًا طويلة ومتعبة. تطلبت رحلات متكررة من منزلها إلى ناشفيل لبعض الإقامات الطويلة في المستشفى. كان العلاج الكيميائي قاسيًا بشكل خاص، تاركًا لها قرحات في الفم والحلق جعلت الأكل والشرب صعبًا.
“كان الأمر صعبًا ومؤلمًا جدًا بالنسبة لي”، تقول.
وقد فوجئت غراي بعدم الراحة التي شعرت بها في وقت سابق من هذا الشهر عندما دفع فرانغول المكبس على حقنة كبيرة لحقن أكثر من ملياري خلية معدلة في جسدها.
“كان هناك لحظة مخيفة وصعبة بالنسبة لي”، تقول. “لكن بعد ذلك بكيت. لكن كانت دموع سعيدة.”
كانت مسرورة أخيرًا لوجود ما تسميه “الخلايا الخارقة” داخل جسدها.
“هذا ما كل هذا يدور حوله — الخلايا المعدلة. هذه هي الخلايا الخارقة التي ستحدث الفرق بين معاناتي من أزمات ألم فقر الدم المنجلي وعدمها”، تقول غراي.
تأمل أن ينجح العلاج وتتخيل حياة بدون فقر الدم المنجلي:
“أن أستيقظ دون ألم. وأن أكون متعبة فقط لأنني فعلت شيئًا — وليس متعبة بدون سبب. وأن أكون بالخارج، وأقفز على الترامبولين مع أطفالي.
“وأذهب إلى حفلات التخرج والزفاف. وأراهم يكبرون. هذا يعني العالم بالنسبة لي.”
سجّل اليوم أو اتصل للحصول على مزيد من المعلومات
الجمعية الأهلية لأمراض الدم الوراثية في البحرين منذ 1991
العنوان: ص.ب ١١٣٩٩ – مملكة البحرين
حقوق الطبع والنشر ٢٠٢٥ @ الجمعية الاهلية لأمراض الدم الوراثية في البحرين – تم التطوير بواسطة ويب ديزاين البحرين
